
II JORNADAS DE ACTUALIZACIÓN EN ENFERMEDAD INFLAMATORIA INTESTINAL CRÓNICA
Organizada por la Sociedad Asturiana de Patología Digestiva.
(Grupo para el estudio de la Enfermedad Inflamatoria Intestinal Crónica)
Coordina: Dra.Cristina Saro Gismera del Hospital de Cabueñes
en Gijón.
1 de Octubre de 1999 a las 17 horas
Salón de Actos del Hospital de Cabueñes. Gijón
De nuevo nos reunimos para comentar los aspectos mas novedosos y/o conflictivos, en relación con la EIIC. Las más recientes investigaciones tanto en el campo de la genética como en el de la Inmunología, nos permiten hoy ver el futuro próximo del tratamiento de esta enfermedad con más expectativa que en los anteriores 20 años. En los últimos 5 años, han estado disponibles los inmunosupresores y un grupo de corticoides tópicos (Budesonida), en el arsenal terapéutico, que han venido a contribuir positivamente al manejo de la enfermedad complicada. Hoy disponemos de otro grupo de inmuno-moduladores, que merecen ser comentados, y que justifican la presente reunión.
El Dr. Joaquín Hinojosa del Val, trabaja en el Hospital de Sagunto y lleva años dedicado al tratamiento de estos enfermos, habiendo contribuido con numerosos estudios de investigación a un mejor conocimiento de la enfermedad. Desarrollará el tema: Etiopatogenia y Nuevas perspectivas en el tratamiento de las formas complicadas de la EIIC.
El Dr. José Ignacio Fernández-Blanco Hernaiz, trabaja en el Hospital de "La Paz", tiene un profundo conocimiento tanto en los aspectos clínicos como quirúrgicos de esta patología, y muy en especial de la enfermedad perianal, tema que nos expondrá.
Por mi parte, haré la introducción con algunas definiciones de la enfermedad complicada que nos permitan entender las siguientes exposiciones, así como presentaré la epidemiología de estas formas en nuestro medio.
Entendemos como EIIC complicada o de difícil manejo, aquella que no responde o responde mal al tratamiento usual de la enfermedad, que exponemos en el siguiente cuadro.
|
EC Fistulosa EC Perianal CU Aguda Grave; Megacolon. EIIC que no responde o responde mal al tratamiento usual. Cortico-Dependiente Cortico-Refracteria |
Antes de iniciar el tratamiento de estos enfermos, valoramos una serie de circunstancias que se resumen en las siguientes tablas:
|
LOCALIZACIÓN CU |
ACTIVIDAD |
COMPLICACIÓN |
RESPUESTA AL TRATAMIENTO |
|
Proctitis |
Quiescente |
Megacolon |
Completa |
|
C. Distal |
Leve |
Hemorragia |
Incompleta |
|
C. Izquierda |
Moderada |
|
Cortico-Dependiente |
|
C. Extensa |
Grave |
|
Cortico-refractaria |
|
Pancolitis |
Indice Truelove |
|
|
|
LOCALIZACIÓN EC |
TIPO |
ACTIVIDAD |
COMPLICACIÓN |
RESPUESTA AL TTO |
|
Colon |
Inflamatoria |
Leve |
Masa Abdominal |
Completa |
|
Íleon terminal |
Estenosante |
Moderada |
Absceso |
Incompleta |
|
Intestinal |
Mixta |
Grave |
Otras: Estenosis Perforación |
Cortico-Dependiente |
|
Colon+Íleon |
Fistulosa Perianal |
I: CDAI P.Hierro Van Hees |
|
Cortico-refractaria |
EIIC cortico- dependiente. (Munkholm P et al; Gut 1994;35:360-362).
CU: Tras intentar tres veces la retirada corticoidea, aparece de nuevo actividad inflamatoria.
EC: Recidiva durante los 30 días siguientes a la suspensión del tratamiento o durante la fase de retirada del mismo (Prednisona), impidiendo la suspensión del mismo durante un año.
EIIC cortico- refractaria.
Entendemos por EIIC refractaria al tratamiento corticoideo, aquella que en su curso evolutivo, a pesar de un correcto tratamiento con corticoides orales, a dosis completas (1 g/Kg de peso), se mantienen los indices de actividad invariables o con escasa respuesta.
* CU: Persistencia de la enfermedad activa, valorada clínica, bioquímica, endoscopia y/o anatomopatológicamente, tras tratamiento con Sulfasalacina (4 gr/día) y/o 5-ASA (3-4,8 gr/día) con o sin enemas de corticoides (100 g), enemas de 5-ASA (2 gr/noche) y Metil-Prednisolona oral (0,75-1 mg/Kg), durante 4-6 semanas.
* En Proctitis ulcerosa: Falta de respuesta a 5-ASA tópico y corticoides tópicos.
* En brote severo se considera no remisión tras 7 días con Prednisona (1-1,5 mg/Kg/día).
* EC: No existe definición. Para la afectación de Colon, se extrapola la definición de la CU.
Tras el primer brote, solo el 44% alcanza remisión, el resto o son refractarios o son dependientes.
Falsa Cortico-Resistencia:
Error en el diagnóstico.
Valorar si los síntomas son secundarios a:
Alteraciones anatomo-funcionales (del tipo de malabsorción de sales biliares, sobre crecimiento bacteriano, estreñimiento del colon derecho, suboclusión por estenosis fibrosa, abscesos sobreañadidos).
Complicaciones por/ o a pesar del tratamiento especifico (malnutrición, sobre-infección asociada a situación de inmunodepresión como abscesos intra-abdominales o infección por gérmenes específicos: Salmonela, Shigela, Campilobacter, E.Coli, Clostridium, Yersinia, Entamoeba Histolitica, Clamidia, Gonococo, CMV).
Causas genuinas de cortico-resistencia:
Tipo I: Por bloqueo de los receptores (tipo I), es un defecto adquirido, que solo afecta a los receptores de los linfocitos T, por lo que se siguen produciendo efectos secundarios.
Tipo II: Por disminución del número de receptores en todas las celulas del organismo (tipo II), es un defecto genético y no se producen efectos secundarios.
Tipo III: Por producción de auto Ac. anti-lipocortina (tipo III). No se produce el bloqueo del Gen que expresa IK-B. Hay un exceso de producción de NF-KB, por lo que los glucocorticoides no son suficientes para bloquear esta actividad, a pesar de que tienen buena función.
Respuesta al tratamiento:
Respuesta Completa: Descenso de los índices de actividad a valores de inactividad.
Respuesta Incompleta: Descenso de los valores de índices de actividad, pero sin alcanzar cifras de inactividad.
EPIDEMIOLOGÍA DE LAS FORMAS COMPLICADAS EN LA ENFERMEDAD INFLAMATORIA INTESTINAL EN GIJÓN.
El objetivo del estudio ha sido conocer la distribución de las formas graves y complicadas de la EIIC en nuestro medio.
Pacientes y métodos: se trata de un estudio epidemiológico, descriptivo, poblacional, retrospectivo del área V (Gijón), del Principado de Asturias. Incluimos en el estudio 286 enfermos diagnosticados de Colitis ulcerosa (CU) según los criterios de Truelove y 245 enfermos diagnosticados de Enfermedad de crohn (EC), acordes con los criterios de Lennard-Jones. Todos ellos adultos, mayores de 14 años al cierre del estudio y cuyo control se realiza habitualmente en Gijón.
En la CU, se valoran las formas cortico-dependientes según la descripción de Munkholm y cortico- refractarias como aquellas que en su curso evolutivo, a pesar de un correcto tratamiento con corticoides orales, a dosis completas (1 Mg/kg/día), se mantienen los índices de actividad (Truelove-Witts) invariables o con escasa respuesta. Las formas fulminantes, se valoran con el mismo índice.
En la EC evaluamos las formas fistulosas, enfermedad perianal y presencia de masa inflamatoria con o sin absceso abdominal. Se correlacionan estos datos con la extensión de la enfermedad.
COLITIS ULCEROSA. GIJÓN 1998.
(286 Casos)
|
EXTEN. |
CASOS |
FULM |
C.CONTINUA |
INTERMIT |
DEPEN |
RESIST |
|
PROCT. |
49 |
0 |
3 (11.5) |
48 (19.2) |
0 |
1 (4.5) |
|
DISTAL |
85 |
0 |
5 (19.3) |
88 (35.2) |
2 (11.8) |
1 (4.5) |
|
IZQ. |
71 |
0 |
31 (11.5) |
66 (26.4) |
2 (11.8) |
1 (4.5) |
|
EXTEN. |
16 |
2 (20) |
2 (7.7) |
11 (4.4) |
1 (5.7) |
2 (9.1) |
|
PANCO |
65 |
8 (80) |
13 (50) |
37 (14.8) |
11 (64.7) |
17 (79.4) |
|
TOTAL |
286 |
10 (3.5%) |
26 (9.1%) |
250 (87.4%) |
17 (5.9%) |
22 (7.7%) |
COLITIS ULCEROSA: SUBTIPOS. (GIJÓN 1998).
(286 Casos)
|
|
CASOS 286 |
OPERADOS |
EXITUS |
EXITUS Prop.E |
MUERTOS Y OPERADOS |
CORT. RESIST |
CORT. DEPEND |
|
FULMINANT |
10 (3.5%) |
9 (90%) |
5 (50%) |
5 (50%) |
4 (44.5%) |
10 (100%) |
0 |
|
MEGACOLON |
4 (1.39%) |
|
|
|
|
|
|
|
C. CONTINUA |
26 (9.1%) |
7 (26.9%) |
3 (11.5%) |
0 |
0 |
9 (34.6%) |
14 (53.8%) |
|
C.INTERMIT |
250 (87.4%) |
6 (2.4%) |
16 (6.4%) |
3 |
3 (50%) |
3 (1.2%) |
3 (1.2%) |
ENFERMEDAD DE CROHN. GIJÓN 1998.
( 245 Casos)
|
EXTENSION |
CASOS |
EXI |
CIR. |
nº Q |
Inflamat 68 (27.6%)
|
Obstruct 21 (8.8%) |
Mixto 156 (63.6%) |
|
Colon |
30 |
2 |
13 |
29 |
25 (83.3%) |
0 |
5 (16.7%) |
|
Íleon Termin |
71 |
2 |
46 |
72 |
43 (20%) |
21 (10 %) |
151 (70 %) |
|
Intestinal |
26 |
2 |
12 |
19 |
|||
|
C+intestinal |
118 |
5 |
84 |
163 |
|||
|
EGD |
13 |
0 |
6 |
16 |
|
|
|
|
Perianal |
87 (35.5%) |
3 |
51 |
84 |
|
|
|
|
Fist.Ent-E-C |
23 (9.38%) |
3 |
17 |
41 |
|
|
|
ENFERMEDAD DE CROHN. GIJÓN 1998
(245 CASOS)
|
EXTENSIÓN. |
EC ( % ) |
FISTULOSA |
MASA ABDOMINAL |
PERIANAL |
|
COLON |
30 (12.3) |
0 |
0 |
|
|
ÍLEON |
71 (29) |
19 (82%) |
92 (81.4%) |
|
|
INTESTINAL |
26 (10.6) |
2 |
4 |
|
|
COLON+INTEST |
118 (48.1) |
2 |
17 |
|
|
TOTAL |
245 |
23 (9.4%) |
113 (46%) |
87 (35.5%) |
E. Fistulosa: p=0.000; Masa Abdominal: p=0.000; E. Perianal: p=NS.
ENF. CROHN. Masa Inflamatoria. Gijón 1998.
(245 Casos)
|
Masa Inflamatoria |
TIPO |
CASOS |
CIRUGÍA |
|
113 ( 46 % ) |
Absceso |
22 ( 9 % ) |
100% |
|
Inflamatorio |
91 ( 37 % ) |
4% |
Conclusiones: a pesar de que la Enfermedad Inflamatoria Intestinal crónica en nuestro medio presenta una prevalencia elevada, las formas complicadas o graves, se presentan en una minoría de ellos y en la CU, significativamente asociada a Pancolitis. En la Enfermedad de Crohn, aparece masa inflamatoria en casi la mitad de los enfermos, pero la presencia de absceso es poco prevalente.
Etiopatogenia de la EIIC. Nuevas perspectivas en el tratamiento de las formas complicadas de la EIIC.
( Dr. Joaquín Hinojosa del Val).
Tanto la etiología como la patogenia de la enfermedad continúan siendo desconocidas, aunque con las más recientes investigaciones, se empieza a vislumbrar y aclarar el origen de la enfermedad, además de reunificar las distintas teorías preexistentes. Cada vez hay más datos para definir la enfermedad como un transtorno genético heredo-transmisible, que favorecida o estimulada la expresión génica por factores externos de diversa índole, tales como infecciones bacterianas o virales, ambiente perinatal, alergia o toxicidad alimentaria, situaciones de stress, o factores trombogénicos como el tabaco o los anovulatorios, provocarían una anómala expresión de las proteínas y/o células encargadas de los mecanismos complejos de la inflamación y de la difusión en las membranas celulares de la pared del intestino.
|
FACTOR INTRÍNSECO
Alteración Genética
Alt. Mecanismos Inflamación Alt. de la permeabilidad de las membranas |
FACTOR EXTRÍNSECO
Infección Dieta Influencia Perinatal AINE F. Trombogénico: Tabaco Anticonceptivos Alt. Psicosocial |
|
ACTIVAN ANÓMALA RESPUESTA INMUNE
(P-ANCAS, HLA, INF, TNF...) |
|
ESTIMULO DE CEL. MUCOSAS INTESTINALES
( Endoteliales y Fagociticas ) |
|
LESIÓN CELULAR - ULCERAS - INFLAMACIÓN
EIIC |
En la patogénesis de la enfermedad, existe una interacción entre factores extrinsecos (medio-ambientales) y factores intrínsecos, de tal forma, que ante un factor medio-ambiental desconocido, la predisposición genética, condicionaría una anómala respuesta inmune que activaría los mecanismos de la inflamación en forma errónea.
FACTORES INTRÍNSECOS
La incorporación de la biología molecular al estudio de la etiopatogenia de la EIIC nos ha permitido conocer la contribución genética al desarrollo de la enfermedad, permitiendo identificar locus responsables en al menos dos cromosomas, pero con gran heterogeneidad que explica las variaciones en el comportamiento de la enfermedad en los diferentes sujetos, tanto en la expresión clínica como en la extensión. En los próximos años, nuevas investigaciones nos permitirán, a través de estudio genético de los genes encausados en la actualidad, no solo conocer futuros candidatos a padecer la enfermedad, sino valorar subgrupos de enfermedad, severidad, respuesta al tratamiento y extensión. Posiblemente también pueda controlarse la enfermedad mediante terapia génica.
Esta alteración genética induciría a una alteración en la regulación de la inmunidad de la mucosa intestinal, alteración en la difusión de las membranas y de la autoinmunidad que puede deberse a cambios estructurales del epitelio, bien por anomalías de las mucoglicoproteinas (de base genética) o por incorporación de proteínas bacterianas o virales, lo que condiciona la modificación de su configuración antigénica y su anómala respuesta ante antígenos no habituales.

El TNF Ky beta(Factor de Necrosis Tumoral), son proteinas preactivadas (precisan activación enzimatica, perdiendo una parte de su cadena), que son producidas por los monocitos macrófagos y también es inducido por linfocitos y células Natural Keler (NK). Se demuestra en forma circulante por todo el organismo y tambien unido a la celula efectora. Todas las celulas del organismo tienen recptores para TNF-alfa y beta. Uniendose a este receptor, inducen a la lisis de la célula receptora. Tiene capacidad para inducir fiebre, leucopenia y necrosis tisular. Se encuentra elevado en la EIIC, tanto circulante como unido a los leucocitos de la pared intestinal.
Tiene una función de regulación de la respuesta inmune y expande esta respuesta inflamatoria a todo el organismo. TNF y también IL-1, inducen el comienzo de la respuesta inflamatoria, provocando la expansión de la respuesta a otras células. El TNF, aumenta en el contexto de todas las inflamaciones. Al bloquear el TNF, se revierte la inflamación. Si se suprime en ratones el gen que expresa el TNF, no se logra inducir la enfermedad inflamatoria en los animales de experimentación. Modula la producción de citocinas (IL-1, IL-6), con lo que potencia el proceso de la inflamación. Estimula la migración linfocitaria mediante el aumento de la permeabilidad de la membrana celular endotelial, y de la expresión de moléculas de adhesión en las células endoteliales y en los leucocitos. Activa la función de neutrofilos y eosinófilos. Induce reactantes de fase aguda y de otras proteinas heáicas. Se demuestra en su forma activa en la pared del intestino y en forma sistémica. (Junto con INF, IL-6 y IL-10).
En la EIIC, las celulas T CD4+ de la lamina propia, cuando son estimuladas, muestran dos patrones distintos de secreción de citocinas o linfocinas: la EC responde con un patron Th1 y la CU responde con patron Th2.
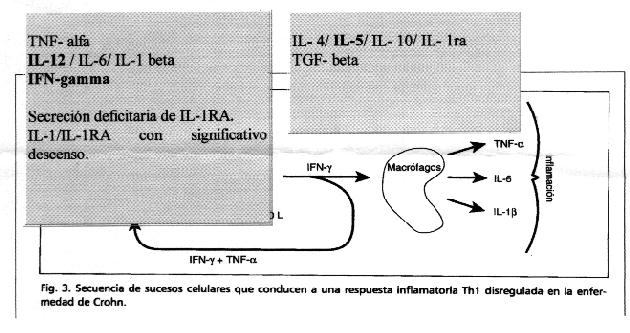
Este patrón de afectación en la EC, es la base para futuros tratamientos de forma que se inhibe o bloquea el patrón Th1, bloqueando los receptores o las moleculas de adhesión, bloqueando la activación de factores intracelulares, bloqueando la transcripción y expresión de genes o bloqueando la síntesis/liberación de TNF-alfa.
Este sistema, solo se ha demostrado en animales de experimentación, pero no en humanos. Se considera que la afectación inflamatoria de la EIIC se produce por un disbalance entre las citocinas pro-inflamatorias y las anti-inflamatorias.
|
LINFOCINAS |
|
|
Pro-inflamatorias |
Anti-inflamatorias |
|
TNF-α, IL-1 beta, IL-8, IL-12, IFN-gamma. |
IL-1ra, IL-4, IL-10, IL-13, TGF beta. |
ANTICUERPOS MONOCLONALES ESPECÍFICOS (Mab).
|
TRATAMIENTO (Situación actual) |
|||
|
|
CITOCINAS |
ANTI-CITOCINAS |
ANTISENSE NUCLEOTIDOS |
|
PRESENTE |
IL-10 (Humano IL-11 recombinante) |
Ac. TNF-α Inhibidores TNF |
ICAM-1 |
|
FUTURO |
|
Ac. IL-1 Ac. IL-1Ra IFN-gamma (dudoso) Ac. IL-12 (dudoso) |
NF K-beta |
Anti -TNF α (Infliximab)(Remicade).
El TNF- α, es una potente citocina proinflamatoria, presente en exceso en la mucosa intestinal de los pacientes con EC activa. El anticuerpo quimérico A2 es un anticuerpo monoclonal que se une con gran afinidad y especificidad al TNF-α humano. Reduce la infiltración de células inflamatorias y la producción de TNF-α en las áreas inflamadas del intestino, reduciendo la proporción de células mononucleares de la lamina propia capaces de expresar TNF-α e Interferon gamma, disminuyendo los niveles de IL-6 y proteína C reactiva. Farmacológicamente, se puede inhibir su liberación (Pentoxifilina) o su unión selectiva al receptor específico.
Dos ensayos controlados, uno en 108 EC moderada-severa y otro en 94 EC fistulosa, se mostraron eficaces en el 82% (16% placebo) del primer estudio y en el 68% (26% placebo) del segundo estudio. Respuesta en 2-3 semanas, con duración de la respuesta de 12 semanas. Reaparecen fistulas en el 15% de los pacientes tratados.
Indicaciones: EC moderada-severa con respuesta inadecuada a tratamiento convencional.
EC fistulosa.
Efectos secundarios: a larga, aun por determinar. En los ensayos: desarrollo de anticuerpos antiquiméricos (HACA) en 1/40 tratados, con reacciones urticariales y posible shock anafiláctico. Posible aumento de infecciones aunque no se ha demostrado esta situación por encima de los controles con placebo, no habiendo aparecido gérmenes oportunistas. Se ha comunicado la aparición de linfoma, no atribuible al fármaco. Síndrome lupoide. Síndrome gripal asociado a la infusión.
Dosis: EC: 5 mg/Kg. Una sola dosis.
Enfermedad fistulosa: 5 mg/Kg. Tres dosis semanas 0-2 y 6.
Probablemente, la dosificación correcta, será de una infusión de 5 mg/Kg, cada 12 semanas, aun no aprobado.
Descripción y Tratamiento de la Enfermedad Perianal.
(Dr. José Ignacio Fernández-Blanco Hernaiz).
Las manifestaciones o complicaciones ano-perineales de la enfermedad de Crohn (E.C.), son desde el punto de vista anatomo patológico las mismas que presenta la enfermedad en otros segmentos: edema, fisuras, úlceras, abscesos, fístulas y estenosis. La especificidad de la enfermedad, viene dada por la especial anatomía y funcionalismo de la zona afecta.
Clásicamente se agrupaban las lesiones del conducto anal y las lesiones perianales en un mismo concepto como lesiones perianal y perineal. Es desde 1992, con los trabajos del grupo de Cardiff, donde se empieza a hablar de enfermedad ano-perianal (EPA) y se utiliza una clasificación uniforme.
|
Ulcera (U) |
0-Ausente |
|
|
1-Superficial (U1) |
a-Anterior o Posterior |
|
|
b-Lateral |
||
|
c-Con Colgajos cutáneos |
||
|
2-Cavitada (U2) |
a-Canal Anal |
|
|
b-Recto inferior |
||
|
c-Extensión a piel Perineal |
||
|
Fistula/Absceso (F) |
0-Ausente |
|
|
1-Baja/superficial (F1) |
a-Perianal |
|
|
b-Ano-vulvar/Ano-escrotal |
||
|
c-Inter-esfinteriana |
||
|
d-Ano-vaginal |
||
|
2-Alta/Compleja (F2) |
a-supraelevador |
|
|
b-Alta directa |
||
|
c-Alta compleja |
||
|
d-Recto-vaginal |
||
|
e-Íleo-perineal |
||
|
Estenosis (S) |
0-Ausente |
|
|
1-Reversible (S1) |
a-Espasmo Canal Anal |
|
|
b-Membranosa (recto distal) |
||
|
c-Espasmo doloroso sin sepsis |
||
|
2-Irreversible (Extraluminal) (S2) |
a-Estenosis anal |
|
|
b-Estenosis rectal |
||
Clasificación Subsidiaria.
|
Patología Anal Asociada (Similar a pacientes sin E.C.) (A) |
0-Ausente |
|
|
1-Hemorroides |
||
|
2-Tumoración (AdenoCa- Escamoso) |
||
|
3-Lesión dermatológica |
||
|
4-Otras |
||
|
5-Cirugía previa |
||
|
EXTENSIÓN Y ACTIVIDAD INTESTINAL
Enfermedad Proximal (P) |
0-Ausente |
|
|
1-Afectación Rectal |
a-Activa |
|
|
b-Inactiva |
||
|
c-No concluyente |
||
|
2-Afectación de Colon (sin lesión en recto) |
a-Activa |
|
|
b-Inactiva |
||
|
c-No concluyente |
||
|
3-Afectación Intestinal |
a-Activa |
|
|
b-Inactiva |
||
|
c-No concluyente |
||
|
4-Investigación Incompleta |
||
|
ACTIVIDAD ANAL
Lesiones Anales Activas (D) |
1-Activa |
|
|
2-Inactiva |
a-Sin secuelas |
|
|
b-Con secuelas |
||
|
3-Supuración aislada |
||
|
4-No concluyente |
||
Los síntomas, se suelen manifestar en el contexto general del complejo sintomático de la E.C. intestinal, solo en pocas ocasiones (8-30%), puede preceder a las manifestaciones intestinales. En esta circunstancia es generalmente dificil diferenciar de lesiones identicas no asociadas a E.C., solo pocos datos diferenciales nos ayudan, tales como la inexistencia de dolor en presencia de una fisura-ulcera anal o la presencia de estenosis anal sin cirugía previa. Siempre conlleva un a importante perdida de la calidad de vida.
Es imprescindible valorar la actividad y extensión de la E.C. intestinal, ya que la mayoría de las veces, la EPA depende de estas lesiones primarias, y su tratamiento tiene como base el tratamiento de las lesiones primarias. Valorar la actividad de la EPA mediante Índices de actividad estándar tiene interés no solo clínico, sino tambien para valorar la efectividad de los distintos tratamientos y llegar a consensos en la epidemiología de la enfermedad. Utilizamos el Índice de Irvine (Universidad de McMaster), por ser el que mejor se correlaciona con la actividad de las lesiones y con la respuesta a los tratamientos.
Los objetivos del tratamiento son: obtener la mejoría de los síntomas y evitar complicaciones en el futuro. En cualquier caso el tratamiento siempre es individualizado para cada enfermo, manteniendo unos principios básicos: no operar enfermos asintomáticos, evitar tanto la incontinencia fecal como aumentar el riesgo de complicaciones que obliguen a la resección del recto. Debe tenerse en cuenta que la simple desviación del transito anal mediante un estoma proximal no cambia el curso evolutivo de las lesiones, por lo que no está indicado con este objetivo, además la aparición de cáncer rectal en estos tramos excluidos es mayor y pasan más desapercibidos, diagnosticandose con retraso y con ello empeorando el pronostico. Insistimos en que es fundamental valorar la extensión y actividad de la enfermedad Intestinal, que debe ser tratada concomitantemente con la EPA .
Utilizamos la clasificación de Cardiff para proponer tratamiento.
Las ulceras profundas (U2), lesiones agresivas, máxime si se asocian con lesiones en recto (P1), no deben tratarse quirúrgicamente, solo utilizamos medidas conservadoras, o en casos extremos, realizamos derivación proximal. Suelen asociarse con importante actividad inflamatoria intestinal, cortico dependencia o cortico-refractariedad, precisando tratamiento con inmunosupresión (Azatrioprina).
Las úlceras superficiales (U1), evolucionan bien con tratamiento médico convencional, e incluso, en ausencia de lesiones musculares y fracaso terapéutico pueden ser subsidiarias de tratamiento quirúrgico (esfinterotomía lateral interna).
Las fistulas bajas (F1), en las que el tratamiento médico fracase, también pueden ser tratadas en forma quirúrgica, respetando al máximo la musculatura esfinteriana.
Las fistulas altas (F2), que se suelen asociar con afectación rectal (P1), y cuyo tratamiento quirúrgico agresivo suele avocar a fracaso de la cicatrización, con infección asociada y terminar en cirugía derivativa, debe tratarse con respeto, y es más sensato el uso de setones de drenaje prolongados.
Las fistulas recto-vaginales (F2d) sintomáticas precisan tratamiento quirúrgico (colgajo rectal de avance), por vía trans-anal o trans-vaginal en función de la existencia de afección rectal (P1), en cuyo caso se suele asociar a derivación proximal.
Las estenosis reversibles (S1), remiten bien con tratamiento conservador.
Las estenosis irreversibles (S2), precisan dilataciones y en ocasiones cirugía derivativa permanente.
Lesiones asociadas (A).:
Los colgajos cutáneos/Tags: no deben ser intervenidos, salvo en el caso de que por una dificultad en la higiene local favorezcan la aparición de abscesos. Siempre se realizará la cirugía cuando la enfermedad esté en fase quiescente, y a pesar de ello existe alto riesgo de que no lleguen a cicatrizar.
Las hemorroides deben ser tratadas en forma conservadora, con higiene de la zona y pomadas. La cirugía se asocia a la aparición de infección y fistulas que pueden obligar a realizar proctectomía.
Tratamiento médico:
Ulceras profundas (U2) y úlceras superficiales (U1), se tratan igual, con pomadas corticoideas tópicas, corticoides orales, Metronidazol o Ciprofloxacino, y Sulfasalazina o 5-ASA. Cuando requieran cirugía, se añade Metronidazol en el postoperatorio, que favorece la cicatrización y previene la recidiva.
Abscesos: Junto con el drenaje quirúrgico se utilizará Metronidazol 10-20 mg/Kg/día o Ciprofloxacino 1 gr/día. Hasta curación de la lesión. Mínimo 15 días.
Fistulas bajas (F1), se inicia tratamiento con Metronidazol 10-20 mg/Kg/día. En caso de falta de respuesta en un mes, se aumenta la dosis hasta un máximo de 1,5 gr /día, monitorizando los efectos segundarios, fundamentalmente la función renal. Como alternativa usamos Ciprofloxacino 1 gr/día. El tratamiento antibiótico, se mantiene hasta 6 meses si es efectivo.
Tanto en el caso de no respuesta como en la aparición de nuevas fistulas al suspender el tratamiento, o cuando por aparición de efectos secundarios haya que suspender éste, se tratarán con Azatioprina/ 6-Mercaptopurina a dosis de 1,5-2,5 mg/Kg/día. El tiempo de duración de este grupo de fármacos está por establecer, pero en reuniones de consenso hemos llegado al acuerdo de mantener por un mínimo de 4 años, hasta la realización de un estudio prospectivo que está en marcha para valorar de forma objetiva este punto.
Fistulas altas (F2): si tras tratamiento quirúrgico conservador con setones durante 3-12 meses, las fistulas recidivarán, se iniciará tratamiento con Ciclosporina a dosis de 8 mg/Kg/día vía oral.
Las estenosis reversibles (S1), remiten bien con tratamiento conservador. Dilatación anal no forzada con bugías, inicialmente bajo anestesia y posteriormente, el propio enfermo hará dilataciones manuales dos o tres veces por día, hasta pasar sin problemas el dedo índice. Si no se obtiene buena respuesta, se indica la exeresis rectal.
Se ensaya un nuevo tratamiento de la enfermedad fistulosa, que incluye la enfermedad perianal fistulosa. El anticuerpo quimérico A2 (Infliximab), es un anticuerpo monoclonal que se une con gran afinidad y especificidad al TNF alfa humano, neutralizando su actividad biológica. Se ha ensayado con seguridad en 200 pacientes con E.C. La pauta de tratamiento son tres dosis de 5 mg/Kg en las semanas 0, 2 y 6. Con esta pauta, el 67.7% de los pacientes cierran sus fistulas, frente al 22% del grupo placebo 14 . EL mayor problema se plantea en el 13% de los enfermos que desarrollan anticuerpos antiquiméricos humano (HACA) y que no podrán ser retratados por riesgo de schok anafiláctico. Algunos recidivan a partir de los 12 meses.
Tratamiento coadyuvante de las lesiones intestinales, se realizará según las pautas clásicas, con corticoides en caso de ser respondedor (Dosis máxima útil: 1 gr/Kg/Día de prednisona). Si el paciente es cortico dependiente o cortico refractario, utilizamos Inmunomoduladores: Azatioprina / 6-Mercaptopurina a dosis de 1,5-2,5 mg/Kg/día.
ACCU ACTUAL Nro.22
Asturias - Octubre de 1999
